Função orgânica dos hidrocarbonetos
Hidrocarboneto, qualquer de uma classe de compostos químicos orgânicos compostos apenas dos elementos carbono (C) e hidrogênio (H). Os átomos de carbono se unem para formar a estrutura do composto, e os átomos de hidrogênio se ligam a eles em muitas configurações diferentes. Os hidrocarbonetos são os principais constituintes do petróleo e do gás natural. Eles servem como combustíveis e lubrificantes, bem como matérias-primas para a produção de plásticos, fibras, borrachas, solventes, explosivos e produtos químicos industriais.
O que é um hidrocarboneto?
Os hidrocarbonetos são compostos orgânicos contendo apenas carbono e hidrogênio. Eles incluem alcanos, alcenos, alcinos e aromáticos. Os últimos três são considerados tipos diferentes de grupos funcionais. Os alcanos geralmente não são considerados como grupos funcionais; em vez disso, um alcano é um composto que não possui grupos funcionais.
Leia também
O grupo funcional em um alceno é uma ligação dupla carbono-carbono. O grupo funcional em um alcino é uma ligação tripla carbono-carbono. Aromáticos são estruturas cíclicas que são planas, totalmente conjugadas e que possuem um número ímpar de pares de elétrons no sistema de ligação π.
Nomenclatura dos hidrocarbonetos
É útil conhecer os nomes dos hidrocarbonetos normais (de cadeia linear), nos quais as cadeias retas de hidrocarbonetos estão ligadas por ligações simples e as valências dos carbonos estão saturadas com hidrogênios. Os nomes destes compostos formam os nomes de raiz de outros compostos tendo o mesmo número de átomos de carbono numa cadeia contínua. Se o hidrogênio final em uma dessas cadeias é substituído por outro átomo, a cadeia é descrita como um grupo substituinte, como nas seguintes fórmulas:
1 CH4 metano CH3-metil
2 CH3CH3 etano CH3CH2-etilo
3 CH3CH2CH3 propano CH3CH2CH2-propilo
4 butano CH3CH2CH2CH3 CH3CH2CH2CH2-butilo
5 CH3CH2CH2CH2CH3 pentano CH3CH2CH2CH2CH2-pentilo
6 CH3CH2CH2CH2CH2CH3 hexano CH3CH2CH2CH2CH2CH2- hexilo
7 CH3CH2CH2CH2CH2CH2CH3 heptano CH3CH2CH2CH2CH2CH2CH2- heptilo
8 CH3CH2CH2CH2CH2CH2CH2CH3 octano CH3CH2CH2CH2CH2CH2CH2CH2- octilo
9 CH3CH2CH2CH2CH2CH2CH2CH2CH3 nonano CH3CH2CH2CH2CH2CH2CH2CH2CH2-nonilo
10 CH3CH2CH2CH2CH2CH2CH2CH2CH2CH3 decano CH3CH2CH2CH2CH2CH2CH2CH2CH2CH2-decil
Os nomes de alcenos e alcinos baseiam-se nos nomes dos alcanos, mas o sufixo do nome varia para indicar o grupo funcional presente. Por exemplo, um composto de dois carbonos contendo uma ligação dupla, CH2 = CH2, é chamado eteno em vez de etano.
Alcano C-C contém apenas ligações simples carbono-carbono, com sufixo ano
Alceno C = C contém uma ligação dupla carbono-carbono, com sufixo eno
Alcino C = C contém uma ligação tripla carbono-carbono, com sufixo ino
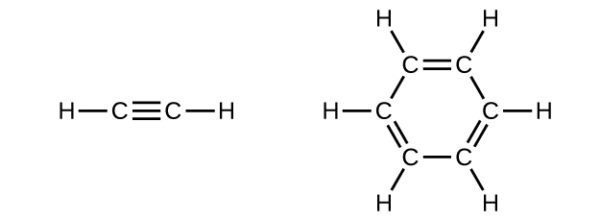
Entenda os hidrocarbonetos e conheça melhor seus usos na química orgânica. (Foto: BC Open Textbooks)
Química dos Hidrocarbonetos alcanos
Em química orgânica, um alcano, ou parafina (um nome histórico que também tem outros significados), é um hidrocarboneto saturado acíclico. Em outras palavras, um alcano consiste em átomos de hidrogênio e carbono dispostos em uma estrutura de árvore na qual todas as ligações carbono-carbono são únicas.
Os alcanos possuem a fórmula química geral CnH2n + 2. Os alcanos variam em complexidade do caso mais simples de metano (CH4), onde n = 1 (algumas vezes chamado de molécula parental), para moléculas arbitrariamente grandes e complexas, como pentacontano (C50H102) ou 6-etil-2-metil-5- (1-metiletil) octano, um isômero do tetradecano (C14H30)
A IUPAC define alcanos como hidrocarbonetos acíclicos ramificados ou não ramificados tendo a fórmula geral CnH2n + 2 e, portanto, consistindo inteiramente de átomos de hidrogênio e átomos de carbono saturados. No entanto, algumas fontes utilizam o termo para designar qualquer hidrocarboneto saturado, incluindo aqueles que são monocíclicos (isto é, os cicloalcanos) ou policíclicos, apesar de terem uma fórmula geral diferente (isto é, os cicloalcanos são CnH2n).
Em um alcano, cada átomo de carbono é sp3-hibridizado com ligações 4-sigma (C-C ou C-H), e cada átomo de hidrogênio é unido a um dos átomos de carbono (em uma ligação C-H). A série mais longa de átomos de carbono ligados em uma molécula é conhecida como seu esqueleto de carbono ou espinha dorsal de carbono. O número de átomos de carbono pode ser considerado como o tamanho do alcano.
Um grupo dos alcanos superiores são as ceras, sólidos à temperatura e pressão ambiente padrão, para os quais o número de carbonos no esqueleto de carbono é maior que cerca de 17. Com suas unidades –CH2 repetidas, os alcanos constituem uma série homóloga de compostos orgânicos nos quais os membros diferem em massa molecular em múltiplos de 14,03u (a massa total de cada uma dessas unidades de ponte de metileno, que compreende um único átomo de carbono de massa 12,01u e dois átomos de hidrogênio de massa aproximada de 1,01u cada).
Os alcanos não são muito reativos e tem pouca atividade biológica. Eles podem ser vistos como árvores moleculares sobre as quais podem ser pendurados os grupos funcionais mais ativos / reativos de moléculas biológicas.
Os alcanos possuem duas fontes comerciais principais: petróleo e gás natural.
Um grupo alquilo, geralmente abreviado com o símbolo R, é um grupo funcional que, como um alcano, consiste unicamente em átomos de carbono e hidrogênio ligados unicamente ligados aciclicamente, por exemplo, um grupo metila ou etila.
Química dos Hidrocarbonetos alcenos
Em química orgânica, um alceno é um hidrocarboneto insaturado que contém pelo menos uma ligação dupla carbono-carbono. As palavras alceno e olefina são frequentemente usadas de forma intercambiável (veja a seção de nomenclatura abaixo). Os alcenos acíclicos, com apenas uma ligação dupla e nenhum outro grupo funcional, conhecido como mono-enes, formam uma série homóloga de hidrocarbonetos com a fórmula geral CnH2n. [2] Os alcenos têm dois átomos de hidrogênio menos que o alcano correspondente (com o mesmo número de átomos de carbono). O alceno mais simples é o etileno (C2H4), denominado eteno pela IUPAC, e é o composto orgânico produzido em larga escala industrialmente. Compostos aromáticos são frequentemente desenhados como alcenos cíclicos, mas sua estrutura e propriedades são diferentes e não são consideradas alcenos.
Química dos Hidrocarbonetos alcinos
Na química orgânica, um alcino é um hidrocarboneto insaturado contendo pelo menos uma ligação tripla carbono-carbono. Os alcinos acíclicos mais simples com apenas uma ligação tripla e nenhum outro grupo funcional formam uma série homóloga com a fórmula química geral CnH2n-2. Os alcinos são tradicionalmente conhecidos como acetilenos, embora o nome acetileno também se refira especificamente ao C2H2, conhecido formalmente como etino, usando a nomenclatura IUPAC. Como outros hidrocarbonetos, os alcinos geralmente são hidrofóbicos, mas tendem a ser mais reativos.
Os alcinos são caracteristicamente mais insaturados do que os alcenos. Assim, eles adicionam dois equivalentes de bromo, enquanto um alceno adiciona apenas um equivalente na reação. Outras reações estão listadas abaixo. Em algumas reações, os alcinos são menos reativos que os alcenos. Por exemplo, em uma molécula com um grupo -eno e um -ino, a adição ocorre preferencialmente no -eno. Possíveis explicações envolvem as duas ligações π na localização do alcalino, o que reduziria a energia do sistema π ou a estabilidade dos intermediários durante a reação. Eles mostram uma maior tendência a polimerizar ou oligomerizar do que os alcenos. Os polímeros resultantes, chamados poliacetilenos (que não contêm unidades alcinosas) são conjugados e podem exibir propriedades semicondutoras.
Alcinos ocorrem em alguns produtos farmacêuticos, incluindo o noretinodrel contraceptivo. Uma ligação tripla carbono-carbono também está presente em medicamentos comercializados, como o antirretroviral Efavirenz e o antifúngico terbinafina. Certas moléculas apresentam um anel contendo um alceno (“ene”) entre dois grupos alcinos (“diino”). Estes compostos são algumas das drogas antitumorais mais agressivas conhecidas, tanto que a subunidade ene-diina é por vezes referida como uma “ogiva”. Ene-diinas sofrem rearranjo através da ciclização de Bergman, gerando intermediários radicais altamente reativos que atacam o DNA dentro do tumor.
Ficou alguma dúvida sobre os hidrocarbonetos? Deixem nos comentários suas perguntas!
Sobre o autor
André é formado em pedagogia, já tendo dado aulas na educação infantil e atuado como professor e coordenador de cursos de inglês. Entendendo como funciona o processo de aprendizagem, decidiu escrever para o blog Múltipla Escolha onde postagens sobre aprendizado, provas, concursos, e muito mais para ajudar seus leitores a aprenderem.
Veja também
O que é número atômico?
O que é equação química?

O que são funções inorgânicas?

Qual a classificação das proteínas?